Yin-Jie Ao a , Yan Yi a , Guo-Hui Wu b, *
Thông tin tác giả
Mã số PMC: PMC10939544
Tóm tắt
Axit poly-L-lactin (PLLA) đã được sử dụng rộng rãi trong lĩnh vực y sinh học. Năm 2004, với tư cách là một vật liệu tiêm, PLLA đã được FDA chấp thuận để điều trị chứng teo cơ mặt liên quan đến AIDS. Kể từ đó, một số chất tiêm có chứa PLLA đã được chấp thuận để tiếp thị ở nhiều quốc gia và khu vực khác nhau. Gần đây, PLLA thường được sử dụng để điều trị các vấn đề trẻ hóa khuôn mặt như vết lõm da và nếp nhăn tĩnh, những thứ luôn gây ra biểu cảm khuôn mặt không như mong muốn. Bài đánh giá này giới thiệu các đặc tính lý hóa, cơ chế kích thích tái tạo, ứng dụng trong thẩm mỹ và bệnh đi kèm khi tiêm của PLLA.
Từ khóa: ứng dụng, axit Poly-L-lactin (PLLA), trẻ hóa
1. Giới thiệu
Năm 1954, các nhà hóa học người Pháp đã phát minh ra chất làm đầy tiêm có khả năng hấp thụ, bán vĩnh viễn, tương thích sinh học và có quán tính miễn dịch. [ 1 , 2 ] Các nước châu Âu đã áp dụng PLLA sớm hơn và hiện nay đã đạt được thương mại hóa hoàn thiện. [ 3 ] Các thương hiệu chất làm đầy PLLA chủ yếu bao gồm Sculptra (Pháp), Derma Veil (Mỹ), AestheFill (Hàn Quốc), Rebron (Trung Quốc), EVOPLLA (Trung Quốc), v.v. [ 4 – 6 ] Seulptra là thương hiệu uy tín nhất trong số đó. [ 7 ] Năm 2004, Sculptra đã được FDA chấp thuận để điều trị chứng teo mỡ mặt liên quan đến AIDS. [ 8 ] Năm 2009, nó được chấp thuận để điều trị nếp nhăn do tuổi tác. [ 9 ] Năm 2021, chất làm đầy PLLA trong nước đã được Cục Quản lý Sản phẩm Y tế Quốc gia Trung Quốc chấp thuận để đưa ra thị trường. Trong các lĩnh vực y học khác, PLLA cũng được sử dụng làm vật liệu để sản xuất chỉ khâu hấp thụ, dụng cụ cố định chỉnh hình, stent niệu đạo và khí quản, cấy ghép nha khoa và vật mang vắc-xin. [ 10 , 11 ] Trong da liễu, PLLA có thể được ứng dụng trong các khía cạnh trẻ hóa khuôn mặt như làm đầy thể tích khuôn mặt, phẫu thuật sẹo và làm giảm nếp nhăn thông qua kích thích tái tạo collagen. [ 12 , 13 ] Theo Vleggaar D, PLLA có thể thúc đẩy tái tạo collagen và được chuyển hóa thành carbon dioxide và nước từ từ. [ 14 ] Các nghiên cứu gần đây đã phát hiện ra rằng ngay cả khi PLLA ban đầu bị phân hủy hoàn toàn, các sợi collagen tái tạo vẫn có thể hoạt động trong một thời gian dài. [ 15 ] Vật liệu này có hiệu quả lâu dài và mức độ an toàn và hài lòng cao. [ 2 ]
2. Tính chất lý hóa của PLLA
Axit polylactic (PLA) là một axit poly-α-hydroxy được tổng hợp từ axit lactic (LA) tồn tại ở 2 đồng phân lập thể quang học có hoạt tính, cụ thể là L-LA và D-LA (S và R theo cấu hình tuyệt đối tương ứng). [ 16 ] Quá trình trùng hợp L- và D-lactide tinh khiết về mặt quang học tạo ra các đồng trùng hợp đẳng hướng của Poly-(L-lactide) (PLLA) và Poly-(D-Lactide), tương ứng. [ 16 ] Hiện nay, PLLA là vật liệu chính của dòng PLA trên thị trường thẩm mỹ y tế. [ 7 ] Vật liệu PLLA dạng tiêm thường là bột đông khô chứa các hạt vi mô PLLA (Hình 1 ). [ 7 ] Lấy Sculptra làm ví dụ, mỗi lọ Sculptra kết hợp các hạt vi mô PLLA, carboxymethylcellulose và mannitol không gây sốt, các thành phần còn lại có thể được hưởng lợi từ tính ổn định của các hạt vi mô cũng như giảm sưng sau khi tiêm. [ 7 ] Là một thành viên của axit alpha-hydroxy, PLLA là một loại polyme không độc hại và dễ hấp thụ với trọng lượng phân tử từ 40kDa đến 50kDa. [ 17 ] Cần phải tái huyền phù bằng 3-5ml nước muối và tiêm xong trong vòng 72 giờ. [ 17 ] Đáng chú ý là trọng lượng phân tử của PLLA không chỉ có thể ngăn ngừa nó bị thực bào bởi các đại thực bào da và mao mạch mà còn giúp các bác sĩ lâm sàng tiêm dễ dàng hơn bằng ống tiêm 27G. [ 14 , 18 ] Hiệu ứng làm đầy tức thời của PLLA sẽ mất dần sau 1 tuần khi dung môi được hấp thụ. [ 17 ] Tuy nhiên, các vi hạt PLLA còn lại sẽ được bao bọc bởi các đại thực bào tăng sinh do tình trạng viêm dưới lâm sàng của dị vật (Hình 2 ). [ 19 ] Theo Gottfried et al, các hạt vi mô PLLA vẫn được bao bọc bởi tế bào lympho và đại thực bào 3 tháng sau khi tiêm. [ 20 ] PLLA sẽ bị phân hủy thành LA và sau đó được chuyển hóa thành carbon dioxide và nước, hoặc được tổng hợp bằng glucose. [ 19 ] Brady JM cũng tìm ra chất chuyển hóa cuối cùng của PLLA là nước và carbon dioxide, và chuỗi phản ứng là không thể đảo ngược. [ 19 ] Thông qua các thí nghiệm trên động vật gặm nhấm, Brady JM đã xác minh PLLA có thể gây ra sự tăng sinh của tế bào lympho và đại thực bào, do đó kích thích sự tăng sinh của nguyên bào sợi. [ 19 ]Theo Vleggaar D, trong 6 tháng đầu sau khi tiêm, tình trạng viêm do dị vật giảm dần, collagen type I sẽ tăng sinh dần, có thể duy trì trong 2 năm hoặc lâu hơn. [ 14 ]
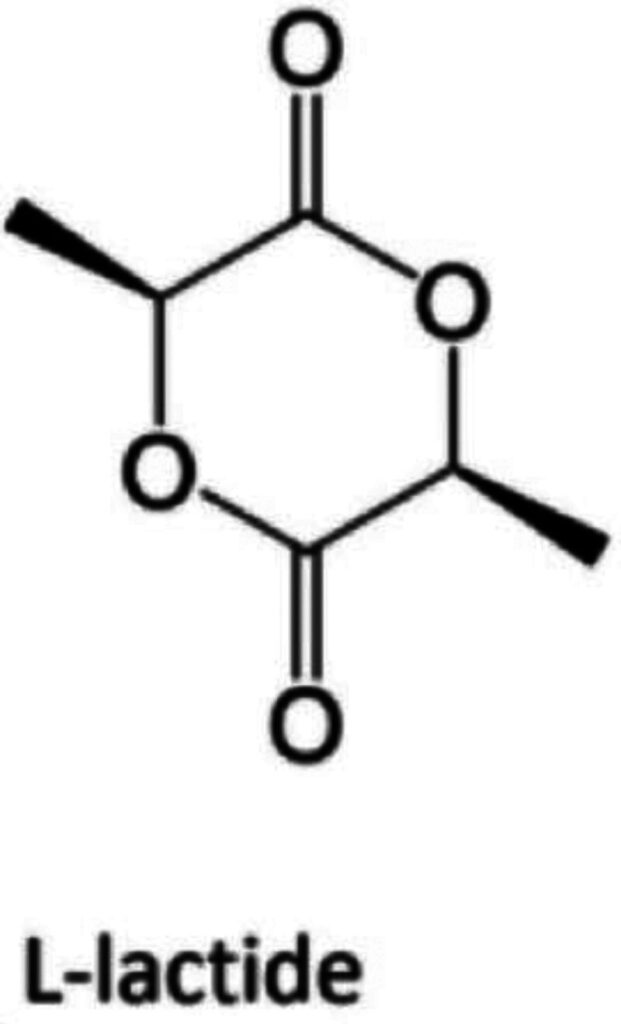
Công thức hóa học của poly-L-lactic.
Chức năng của poly-L-lactic *PLLA: poly-L-lactic.
3. PLLA kích thích sự tăng sinh và tái tạo collagen ở da
Không giống như chất làm đầy truyền thống chỉ dựa vào việc tăng thể tích để đạt được hiệu quả làm đầy, PLLA kích thích sự tăng sinh collagen bằng cách tái tạo nguyên bào sợi. [ 21 ] Hiệu ứng làm đầy tức thì của PLLA sẽ biến mất dần dần từ 3 đến 7 ngày sau khi tiêm khi dung môi được hấp thụ. [ 22 ] Các vi hạt PLLA sẽ xâm chiếm tại chỗ và bắt đầu hoạt động. [ 23 ] 1 tháng sau khi tiêm, các vi hạt PLLA được bao bọc bởi các đại thực bào và tế bào lympho được tạo ra bởi tình trạng viêm do dị vật. [ 24 ] 3 tháng sau khi tiêm, các vi hạt PLLA co lại dần dần và được thủy phân thành PLA hoặc LA. [ 25 ] Sau khi thực bào, các chất chuyển hóa cuối cùng là carbon dioxide và nước. [ 26 ] Phản ứng sẽ kích thích sự tăng sinh của nguyên bào sợi. [ 26 ] Sáu tháng sau khi tiêm, tốc độ tăng sinh của nguyên bào sợi đạt đến đỉnh điểm và bắt đầu tiết ra collagen rất nhiều, chủ yếu là collagen loại I, để làm đầy các mô. [ 27 ] Để tóm tắt chuỗi phản ứng toàn diện, các hạt vi mô PLLA được tiêm sẽ kích hoạt tình trạng viêm dị vật dưới lâm sàng, dẫn đến sự tăng sinh collagen thông qua quá trình xâm chiếm và tái tạo nguyên bào sợi. [ 24 ] Các chất chuyển hóa cuối cùng là carbon dioxide và nước. [ 24 ] Các thí nghiệm trong ống nghiệm cũng đã xác nhận tác dụng kích thích của PLLA đối với quá trình tổng hợp collagen. [ 28 , 29 ] Đáng chú ý là nguyên bào sợi hoạt động như một chất điều hòa sự tăng sinh collagen trong các phản ứng này, điều đó có nghĩa là khi các hạt vi mô PLLA ban đầu được chuyển hóa hoàn toàn, các nguyên bào sợi tái sinh vẫn có thể hoạt động chính xác trong ít nhất 2 năm hoặc lâu hơn. [ 30 ] Hơn nữa, không giống như các vật liệu yếu tố tăng trưởng, trong đó các mô sẽ tăng sinh với tốc độ nhân lên cao trong 10 năm hoặc thậm chí lâu hơn, điều này sẽ dẫn đến kết cục thảm khốc cho hầu hết bệnh nhân. [ 31 ] Sự tăng sinh collagen của PLLA sẽ được các nguyên bào sợi quản lý một cách tinh vi và sau đó cung cấp kết quả nhẹ nhàng và có thể kiểm soát được. [ 32 , 33 ] Ngoài ra, theo Hanako et al, collagen loại III sẽ được tìm thấy 16 tuần sau khi tiêm. [ 34 ] Collagen loại III, vì sản xuất hạn chế ở người lớn, cũng được gọi là “collagen trẻ em”. [35 ] Đồng thời, vì sự phân bố chủ yếu của nó giữa lớp biểu bì và lớp hạ bì, cũng được gọi là “microcollagen”. [ 35 ] Collagen loại III hoạt động như khung đỡ dưới da, liên quan đến sự hình thành các nếp nhăn tĩnh trên bề mặt. [ 36 ] Do đó, PLLA có thể thúc đẩy sự tăng sinh của collagen loại I/III và có lợi cho việc làm mới các nếp nhăn trên da bề mặt. [ 36 ]
4. Ứng dụng của PLLA
PLLA được sử dụng để tăng cường mô, tăng độ dẻo dai của cơ thể, hiệu chỉnh tình trạng da chùng nhão và tái tạo mô collagen ở các vùng như cổ, ngực, mông, bụng, cánh tay trên, đùi, đầu gối và bàn tay do cơ chế tăng sinh mô tự điều chỉnh và tác dụng kéo dài (Bảng 1 ). [ 2 , 12 , 13 ] Trong lĩnh vực trẻ hóa khuôn mặt, PLLA đã được sử dụng trên toàn thế giới trong hơn 18 năm. Các chỉ định của nó bao gồm mở rộng mô, tăng độ dẻo dai cho đường viền, hiệu chỉnh nếp nhăn và teo mô liên quan đến HIV. [ 8 , 37 ] Kể từ khi ứng dụng trong trẻ hóa da, một số thử nghiệm và nghiên cứu lâm sàng đã được tiến hành để đánh giá đầy đủ tính an toàn và hiệu quả của PLLA trên toàn cầu. Li et al đã sử dụng chất làm đầy PLLA mới để điều trị cho những bệnh nhân bị teo mỡ. [ 38 ] Bằng cách đo độ dày của da bằng siêu âm, họ thấy rằng độ dày của da tăng dần. [ 38 ] Một nghiên cứu ở Pháp bao gồm 40 bệnh nhân bị loạn dưỡng mỡ đã sử dụng phần mềm chụp ảnh kỹ thuật số để phân tích ảnh chụp da và phát hiện ra rằng độ dày của da tăng từ 2 đến 6 tháng sau khi tiêm PLLA. [ 39 ] Một nghiên cứu trên 54 bệnh nhân tiêm PLLA tại Hoa Kỳ đã hoàn thành quá trình theo dõi trong 12 tháng. [ 13 ] Sau 12 tháng, độ dày của da tăng 54,9% thông qua phép đo compa. [ 13 ] Theo Moyle và cộng sự và Valantin và cộng sự, PLLA chủ yếu được sử dụng trong thẩm mỹ da và điều trị teo mỡ mặt liên quan đến HIV, không chỉ mang lại kết quả thẩm mỹ tốt mà còn cải thiện chất lượng cuộc sống. [ 40 , 41 ] Năm 2019, Bohnert và cộng sự phát hiện ra rằng điều trị PLLA nhiều lần có thể cải thiện các khiếm khuyết về đường viền cũng như chất lượng da. [ 42 ] Theo Baroni et al và Mojallal et al, PLLA có tác dụng tích cực đến các thông số sinh lý của da như độ ẩm, độ đàn hồi, mất nước qua biểu bì và đánh giá chất lượng da như ban đỏ, sắc tố, kích thước lỗ chân lông, độ sáng và mịn, chủ yếu là do sự tăng sinh của collagen. [ 43 , 44 ] Trước đây, nhiều loại chất làm đầy da luôn tập trung ở axit hyaluronic hoặc chất làm đầy lipo. Năm 1934, Carl Meyer và trợ lý của ông là John Palmer đã phân lập được một loại glycosaminoglycan mới được phát hiện từ thủy tinh mắt bò và đặt tên cho chất này là “axit hyaluronic” (HA). [ 45 ]Hyaluronic acid là một polyme polysaccharide tuyến tính tự nhiên bao gồm các đơn vị diglucan lặp lại của N-acetyl-D-glucosamine và axit D-glucuronic được liên kết bởi các liên kết glycosidic β (1,4) và β (1,3). [ 46 ] Thời gian hoạt động của HA có thể đạt khoảng 1 năm với sự cải tiến của công nghệ liên kết ngang. [ 47 ] Tuy nhiên, HA là chất làm đầy không hoạt động, điều đó có nghĩa là nó sẽ yêu cầu tiêm nhiều lần bất kể nó tồn tại trong bao lâu cho một ống tiêm. [ 48 ] Đồng thời, việc tăng số lần tiêm có thể dẫn đến tỷ lệ cao hình thành u nang tại chỗ và hình dạng rộng cục bộ ở các vùng như cằm, trán và lưng. [ 49 ] Tất cả các vấn đề được đề cập ở trên sẽ ảnh hưởng đến sự hài lòng của bệnh nhân. Đối với việc tiêm mỡ, nghiên cứu mới nhất cho thấy tỷ lệ sống sót của một lần tiêm là 20% -80%. [ 50 ] Theo hiểu biết của chúng tôi, chất béo có thể không phải là chất làm đầy hoàn toàn phù hợp để tạo thể tích chính xác cho khuôn mặt hiện nay. Tiêm quá nhiều là cần thiết để đảm bảo sự sống còn của mỡ tại chỗ, tuy nhiên, điều này có thể làm tăng khả năng tắc mạch. [ 51 ] Hoặc một lượng lớn mỡ sống sót tại chỗ có thể dẫn đến hình thái không đạt yêu cầu. [ 51 ] Các biến chứng khác như hoại tử và vôi hóa các nốt mỡ, cảm giác hạt cũng có thể do tiêm quá nhiều tại chỗ. [ 52 ] Đặc biệt đối với các vùng như glabella, trán, thái dương và quanh ổ mắt, nơi thường xuyên tiêm dưới da hoặc tiêm dưới da. [ 52 ] HA dễ gây ra hiệu ứng Tyndall tại chỗ vì nó chứa tác nhân liên kết chéo. [ 53 ] Trong khi đó, tiêm HA sâu không thể cải thiện chính xác các nếp nhăn nông trên da. [ 53 ] Một số học giả đã báo cáo rằng gel mỡ có thể có lợi cho các nếp nhăn tĩnh nông, nhưng quá trình thu thập gel mỡ phức tạp hơn so với việc mang và sử dụng chất làm đầy thương mại. [ 54 – 56 ] Bên cạnh đó, tiêm gel mỡ cũng bao gồm những tranh cãi liên quan đến việc tiêm mỡ đã đề cập ở trên. Như chúng ta đều biết, các mạch máu phân bố dày đặc ở các vùng như glabella, trán, thái dương và quanh hốc mắt, đặc biệt là ở các mô nông. [ 57 ]Hiện tại, không có báo cáo nào khẳng định rằng có thể tránh tuyệt đối việc tiêm nhầm vào mạch máu ở những vùng này. Do đó, ngay cả những người hành nghề có kinh nghiệm vẫn có nguy cơ tắc mạch liên quan đến HA hoặc tiêm mỡ. Vì PLLA là vật liệu tiêm có chứa tác nhân không liên kết chéo, ngay cả khi tiêm nhầm vào mạch máu, nó cũng hiếm khi gây ra các biến chứng thảm khốc như mù lòa hoặc hoại tử da diện rộng. [ 58 – 60 ] Qua quá trình xem xét tài liệu, chúng tôi vẫn chưa tìm thấy bất kỳ báo cáo nào liên quan đến tình trạng tắc mạch do tiêm PLLA ở những bệnh nhân không nhiễm HIV. [ 61 ] Chỉ có một trường hợp liên quan đến tình trạng tắc mạch PLLA liên quan đến HIV được báo cáo vào năm 2012 và bệnh nhân đã dùng nhiều loại thuốc điều trị HIV trong 10 năm. [ 61 ] Tóm lại, PLLA là vật liệu có độ an toàn cực cao liên quan đến viễn cảnh tắc mạch. Hiện nay, liệu pháp kết hợp PLLA và HA được ủng hộ trong công tác lâm sàng. [ 62 ] HA và các vật liệu tiêm hỗ trợ khác có thể được sử dụng để tăng thể tích ở các khoảng dưới SMAS và khoang mỡ sâu, trong khi tiêm PLLA có thể được sử dụng để sửa đổi bề ngoài và làm mới chính xác. [ 63 ] Cuối cùng, PLLA kết hợp với HA thường có thể đạt được hiệu quả trẻ hóa toàn diện khuôn mặt ở nhiều cấp độ. [ 63 ]
5. Biến chứng của PLLA
Qua quá trình xem xét tài liệu, chúng tôi không tìm thấy báo cáo nào về các biến chứng nghiêm trọng liên quan đến tiêm PLLA ở những bệnh nhân không nhiễm HIV. Theo các báo cáo khác nhau, tỷ lệ xuất hiện các nốt sần và u hạt ở da/dưới da dao động từ 1% đến 44%. [ 64 – 68 ] Tuy nhiên, với sự tiến bộ của công nghệ dược phẩm và công nghệ tiêm, cũng như sự cải thiện của các kỹ năng tiêm lại, khả năng hình thành nốt sần đã giảm đáng kể. [ 60 , 65 , 68 ] Hart và cộng sự không tìm thấy bất kỳ nốt sần ở da/dưới da nào ở 100 bệnh nhân được tiêm PLLA vào ngực. [ 69 ] Các biến chứng tạm thời khác, bao gồm bầm tím, sưng và đau, đã giảm đáng kể trong vòng 2 tuần sau khi tiêm. [ 68 ] Các báo cáo về dị ứng PLLA rất hiếm. [ 70 ]
6. Kết luận
PLLA có tác dụng tốt trong việc cải thiện kết cấu da, tăng độ dày của da và làm mờ nếp nhăn tĩnh, v.v., có triển vọng ứng dụng rộng rãi trong việc trẻ hóa da mặt.
TÀI LIỆU THAM KHẢO
[1].Broder KW, Cohen SR. An overview of permanent and semipermanent fillers. Plast Reconstr Surg. 2006;118(3 Suppl):7S–14S. [DOI] [PubMed] [Google Scholar]
[2].Haddad A, Menezes A, Guarnieri C, et al. Recommendations on the use of injectable poly-L-lactic acid for skin laxity in off-face areas. J Drugs Dermatol. 2019;18:929–35. [PubMed] [Google Scholar]
[3].Alessio R, Rzany B, Eve L, et al. European expert recommendations on the use of injectable poly-L-lactic acid for facial rejuvenation. J Drugs Dermatol. 2014;13:1057–66. [PubMed] [Google Scholar]
[4].Christen MO. Collagen stimulators in body applications: a review focused on Poly-L-Lactic Acid (PLLA). Clin Cosmet Investig Dermatol. 2022;15:997–1019. [DOI] [PMC free article] [PubMed] [Google Scholar]
[5].Vleggaar D, Fitzgerald R, Lorenc ZP, et al. Consensus recommendations on the use of injectable poly-L-lactic acid for facial and nonfacial volumization. J Drugs Dermatol. 2014;13(4 Suppl):s44–51. [PubMed] [Google Scholar]
[6].Vleggaar D, Fitzgerald R, Lorenc ZP. The need for consensus recommendations on the use of injectable poly-L-lactic acid for facial and nonfacial volumization. J Drugs Dermatol. 2014;13(4 Suppl):s28. [PubMed] [Google Scholar]
[7].Lam SM, Azizzadeh B, Graivier M. Injectable poly-L-lactic acid (Sculptra): technical considerations in soft-tissue contouring. Plast Reconstr Surg. 2006;118(3 Suppl):55S–63S. [DOI] [PubMed] [Google Scholar]
[8].Vleggaar D. Soft-tissue augmentation and the role of poly-L-lactic acid. Plast Reconstr Surg. 2006;118(3 Suppl):46S–54S. [DOI] [PubMed] [Google Scholar]
[9].Goldberg D, Guana A, Volk A, et al. Single-arm study for the characterization of human tissue response to injectable poly-L-lactic acid. Dermatol Surg. 2013;39:915–22. [DOI] [PubMed] [Google Scholar]
[10].Wilson AJ, Taglienti AJ, Chang CS, et al. Current applications of facial volumization with fillers. Plast Reconstr Surg. 2016;137:872e–89e. [DOI] [PubMed] [Google Scholar]
[11].Lee JC, Lorenc ZP. Synthetic fillers for facial rejuvenation. Clin Plast Surg. 2016;43:497–503. [DOI] [PubMed] [Google Scholar]
[12].Sickles CK, Nassereddin A, Gross GP. Poly-L-Lactic Acid. In: StatPearls. edn. Treasure Island (FL): StatPearls Publishing; 2024. [PubMed] [Google Scholar]
[13].Jabbar A, Arruda S, Sadick N. Off face usage of poly-L-lactic acid for body rejuvenation. J Drugs Dermatol. 2017;16:489–94. [PubMed] [Google Scholar]
[14].Vleggaar D. Facial volumetric correction with injectable poly-L-lactic acid. Dermatol Surg. 2005;31(11 Pt 2):1511–7; discussion 1517-1518. [DOI] [PubMed] [Google Scholar]
[15].Vleggaar D, Bauer U. Facial enhancement and the European experience with sculptra (poly-l-lactic acid). J Drugs Dermatol. 2004;3:542–7. [PubMed] [Google Scholar]
[16].Cunha BLC, Bahú JO, Xavier LF, et al. Lactide: production routes, properties, and applications. Bioengineering (Basel). 2022;9:164. [DOI] [PMC free article] [PubMed] [Google Scholar]
[17].Moyle GJ, Lysakova L, Brown S, et al. A randomized open-label study of immediate versus delayed polylactic acid injections for the cosmetic management of facial lipoatrophy in persons with HIV infection. HIV Med. 2004;5:82–7. [DOI] [PubMed] [Google Scholar]
[18].Gogolewski S, Jovanovic M, Perren SM, et al. Tissue response and in vivo degradation of selected polyhydroxyacids: polylactides (PLA), poly(3-hydroxybutyrate) (PHB), and poly(3-hydroxybutyrate-co-3-hydroxyvalerate) (PHB/VA). J Biomed Mater Res. 1993;27:1135–48. [DOI] [PubMed] [Google Scholar]
[19].Brady JM, Cutright DE, Miller RA, et al. Resorption rate, route, route of elimination, and ultrastructure of the implant site of polylactic acid in the abdominal wall of the rat. J Biomed Mater Res. 1973;7:155–66. [DOI] [PubMed] [Google Scholar]
[20].Lemperle G, Morhenn V, Charrier U. Human histology and persistence of various injectable filler substances for soft tissue augmentation. Aesthetic Plast Surg. 2020;44:1348–60. [DOI] [PubMed] [Google Scholar]
[21].Mariano M, Pilate F, de Oliveira FB, et al. Preparation of cellulose nanocrystal-reinforced poly(lactic acid) nanocomposites through noncovalent modification with PLLA-based surfactants. ACS Omega. 2017;2:2678–88. [DOI] [PMC free article] [PubMed] [Google Scholar]
[22].Herrmann JL, Hoffmann RK, Ward CE, et al. Biochemistry, physiology, and tissue interactions of contemporary biodegradable injectable dermal fillers. Dermatol Surg. 2018;44:S19–31. [DOI] [PubMed] [Google Scholar]
[23].Sadick NS, Manhas-Bhutani S, Krueger N. A novel approach to structural facial volume replacement. Aesthetic Plast Surg. 2013;37:266–76. [DOI] [PubMed] [Google Scholar]
[24].Cabral LRB, Teixeira LN, Gimenez RP, et al. Effect of hyaluronic acid and poly-L-lactic acid dermal fillers on collagen synthesis: an in vitro and in vivo study. Clin Cosmet Investig Dermatol. 2020;13:701–10. [DOI] [PMC free article] [PubMed] [Google Scholar]
[25].Kontis TC. Contemporary review of injectable facial fillers. JAMA Facial Plast Surg. 2013;15:58–64. [DOI] [PubMed] [Google Scholar]
[26].Fitzgerald R, Bass LM, Goldberg DJ, et al. Physiochemical characteristics of poly-L-lactic acid (PLLA). Aesthet Surg J. 2018;38(suppl_1):S13–7. [DOI] [PubMed] [Google Scholar]
[27].Humble G, Mest D. Soft tissue augmentation using sculptra. Facial Plast Surg. 2004;20:157–63. [DOI] [PubMed] [Google Scholar]
[28].Kim SA, Kim HS, Jung JW, et al. Poly-L-lactic acid increases collagen gene expression and synthesis in cultured dermal fibroblast (Hs68) through the p38 MAPK pathway. Ann Dermatol. 2019;31:97–100. [DOI] [PMC free article] [PubMed] [Google Scholar]
[29].Ray S, Ta HT. Investigating the effect of biomaterials such as poly-(l-Lactic Acid) particles on collagen synthesis in vitro: method is matter. J Funct Biomater. 2020;11:51. [DOI] [PMC free article] [PubMed] [Google Scholar]
[30].Oh H, Lee S, Na J, et al. Comparative evaluation of safety and efficacy of a novel hyaluronic acid-polynucleotide/Poly-L-lactic acid composite dermal filler. Aesthetic Plast Surg. 2021;45:1792–801. [DOI] [PubMed] [Google Scholar]
[31].Liao X, Zhang ZD, Li SH, et al. Facial intramuscular lipoma occurrence following topical cosmetic injection with a mixture of basic fibroblast growth factor: a report of two cases. J Cosmet Laser Ther. 2017;19:303–6. [DOI] [PubMed] [Google Scholar]
[32].Palm M, Chayavichitsilp P. The “skinny”on sculptra: a practical primer to volumization with poly-L-lactic acid. J Drugs Dermatol. 2012;11:1046–52. [PubMed] [Google Scholar]
[33].Breithaupt A, Fitzgerald R. Collagen stimulators: poly-L-lactic acid and calcium hydroxyl apatite. Facial Plast Surg Clin North Am. 2015;23:459–69. [DOI] [PubMed] [Google Scholar]
[34].Nishimoto H, Kokubu T, Inui A, et al. Ligament regeneration using an absorbable stent-shaped poly-L-lactic acid scaffold in a rabbit model. Int Orthop. 2012;36:2379–86. [DOI] [PMC free article] [PubMed] [Google Scholar]
[35].Brown SR, Cleveland EM, Deeken CR, et al. Type I/type III collagen ratio associated with diverticulitis of the colon in young patients. J Surg Res. 2017;207:229–34. [DOI] [PubMed] [Google Scholar]
[36].Chaudhuri RK, Bojanowski K. Bakuchiol: a retinol-like functional compound revealed by gene expression profiling and clinically proven to have anti-aging effects. Int J Cosmet Sci. 2014;36:221–30. [DOI] [PubMed] [Google Scholar]
[37].Vleggaar D, Fitzgerald R, Lorenc ZP. The history behind the use of injectable poly-L-lactic acid for facial and nonfacial volumization: the positive impact of evolving methodology. J Drugs Dermatol. 2014;13(4 Suppl):s32–34. [PubMed] [Google Scholar]
[38].Li A, Long A, Fang R, et al. High-frequency ultrasound for long-term safety assessment of poly-L-lactic acid facial filler. Dermatol Surg. 2022;48:1071–5. [DOI] [PubMed] [Google Scholar]
[39].Lafaurie M, Dolivo M, Girard PM, et al. Polylactic acid vs. polyacrylamide hydrogel for treatment of facial lipoatrophy: a randomized controlled trial [Agence Nationale de Recherches sur le SIDA et les Hépatites Virales (ANRS) 132 SMILE]. HIV Med. 2013;14:410–20. [DOI] [PubMed] [Google Scholar]
[40].Moyle GJ, Brown S, Lysakova L, et al. Long-term safety and efficacy of poly-L-lactic acid in the treatment of HIV-related facial lipoatrophy. HIV Med. 2006;7:181–5. [DOI] [PubMed] [Google Scholar]
[41].Valantin MA, Aubron-Olivier C, Ghosn J, et al. Polylactic acid implants (New-Fill) to correct facial lipoatrophy in HIV-infected patients: results of the open-label study VEGA. AIDS. 2003;17:2471–7. [DOI] [PubMed] [Google Scholar]
[42].Bohnert K, Dorizas A, Lorenc P, et al. Randomized, controlled, multicentered, double-blind investigation of injectable poly-L-lactic acid for improving skin quality. Dermatol Surg. 2019;45:718–24. [DOI] [PubMed] [Google Scholar]
[43].Baroni Edo R, Biondo-Simões Mde L, Auersvald A, et al. Influence of aging on the quality of the skin of white women: the role of collagen. Acta Cir Bras. 2012;27:736–40. [DOI] [PubMed] [Google Scholar]
[44].Mojallal A, Lequeux C, Shipkov C, et al. Improvement of skin quality after fat grafting: clinical observation and an animal study. Plast Reconstr Surg. 2009;124:765–74. [DOI] [PubMed] [Google Scholar]
[45].Pereira H, Sousa DA, Cunha A, et al. Hyaluronic acid. Adv Exp Med Biol. 2018;1059:137–53. [DOI] [PubMed] [Google Scholar]
[46].Gupta RC, Lall R, Srivastava A, et al. Hyaluronic acid: molecular mechanisms and therapeutic trajectory. Front Vet Sci. 2019;6:192. [DOI] [PMC free article] [PubMed] [Google Scholar]
[47].Abatangelo G, Vindigni V, Avruscio G, et al. Hyaluronic acid: redefining its role. Cells. 2020;9:1743. [DOI] [PMC free article] [PubMed] [Google Scholar]
[48].Murthy R, Roos JCP, Goldberg RA. Periocular hyaluronic acid fillers: applications, implications, complications. Curr Opin Ophthalmol. 2019;30:395–400. [DOI] [PubMed] [Google Scholar]
[49].Vidič M, Bartenjev I. An adverse reaction after hyaluronic acid filler application: a case report. Acta Dermatovenerol Alp Pannonica et Adriatica. 2018;27:165–7. [PubMed] [Google Scholar]
[50].Chang CS, Lanni MA, Mirzabeigi MN, et al. Large-volume fat grafting: identifying risk factors for fat necrosis. Plast Reconstr Surg. 2022;150:941e–9e. [DOI] [PubMed] [Google Scholar]
[51].Benslimane F. Personal strategy to avoid fat embolism during fat grafting: brisk withdrawal of cannula while injection. Aesthetic Plast Surg. 2021;45:718–29. [DOI] [PubMed] [Google Scholar]
[52].Liu H, Wu X, Zhang X, et al. Internal carotid artery embolism after autologous fat injection for temporal augmentation. Aesthetic Plast Surg. 2019;43:383–7. [DOI] [PubMed] [Google Scholar]
[53].Rootman DB, Lin JL, Goldberg R. Does the Tyndall effect describe the blue hue periodically observed in subdermal hyaluronic acid gel placement? Ophthal Plast Reconstr Surg. 2014;30:524–7. [DOI] [PubMed] [Google Scholar]
[54].Yang Z, Jin S, He Y, et al. Comparison of microfat, nanofat, and extracellular matrix/stromal vascular fraction gel for skin rejuvenation: basic research and clinical applications. Aesthet Surg J. 2021;41:NP1557–70. [DOI] [PubMed] [Google Scholar]
[55].van Dongen JA, Harmsen MC, Stevens HP, et al. A difference between volume restoration and tissue rejuvenation. Aesthet Surg J. 2021;41:NP1247–8. [DOI] [PMC free article] [PubMed] [Google Scholar]
[56].Tonnard P, Verpaele A, Peeters G, et al. Nanofat grafting: basic research and clinical applications. Plast Reconstr Surg. 2013;132:1017–26. [DOI] [PubMed] [Google Scholar]
[57].Lee KL, Lee HJ, Youn KH, et al. Positional relationship of superior and inferior labial artery by ultrasonography image analysis for safe lip augmentation procedures. Clin Anat. 2020;33:158–64. [DOI] [PubMed] [Google Scholar]
[58].Trinh LN, Gupta A. Non-hyaluronic acid fillers for midface augmentation: a systematic review. Facial Plast Surg. 2021;37:536–42. [DOI] [PubMed] [Google Scholar]
[59].Trinh LN, Grond SE, Gupta A. Dermal fillers for tear trough rejuvenation: a systematic review. Facial Plast Surg. 2022;38:228–39. [DOI] [PubMed] [Google Scholar]
[60].Bartus C, William Hanke C, Daro-Kaftan E. A decade of experience with injectable poly-L-lactic acid: a focus on safety. Dermatol Surg. 2013;39:698–705. [DOI] [PubMed] [Google Scholar]
[61].Roberts SA, Arthurs BP. Severe visual loss and orbital infarction following periorbital aesthetic poly-(L)-lactic acid (PLLA) injection. Ophthal Plast Reconstr Surg. 2012;28:e68–70. [DOI] [PubMed] [Google Scholar]
[62].de Melo F, Carrijo A, Hong K, et al. Minimally invasive aesthetic treatment of the face and neck using combinations of a PCL-based collagen stimulator, PLLA/PLGA suspension sutures, and cross-linked hyaluronic acid. Clin Cosmet Investig Dermatol. 2020;13:333–44. [DOI] [PMC free article] [PubMed] [Google Scholar]
[63].Chuang AD, Yang CK, Chang CC, et al. Cephalometric analysis following combined Sub-SMAS hyaluronic acid injection and subdermal and supraperiosteal poly-L-lactic acid injections in Asian women. J Cosmet Dermatol. 2022;21:2429–36. [DOI] [PMC free article] [PubMed] [Google Scholar]
[64].Fabi SG, Goldman MP. The safety and efficacy of combining poly-L-lactic acid with intense pulsed light in facial rejuvenation: a retrospective study of 90 patients. Dermatol Surg. 2012;38(7 Pt 2):1208–16. [DOI] [PubMed] [Google Scholar]
[65].Levy RM, Redbord KP, Hanke CW. Treatment of HIV lipoatrophy and lipoatrophy of aging with poly-L-lactic acid: a prospective 3-year follow-up study. J Am Acad Dermatol. 2008;59:923–33. [DOI] [PubMed] [Google Scholar]
[66].Schierle CF, Casas LA. Nonsurgical rejuvenation of the aging face with injectable poly-L-lactic acid for restoration of soft tissue volume. Aesthet Surg J. 2011;31:95–109. [DOI] [PubMed] [Google Scholar]
[67].Lowe NJ. Dispelling the myth: appropriate use of poly-L-lactic acid and clinical considerations. J Eur Acad Dermatol Venereol. 2006;20:2–6. [DOI] [PubMed] [Google Scholar]
[68].Redaelli A, Forte R. Cosmetic use of polylactic acid: report of 568 patients. J Cosmet Dermatol. 2009;8:239–48. [DOI] [PubMed] [Google Scholar]
[69].Hart DR, Fabi SG, White WM, et al. Current concepts in the use of PLLA: clinical synergy noted with combined use of microfocused ultrasound and poly-L-lactic acid on the face, neck, and décolletage. Plast Reconstr Surg. 2015;136(5 Suppl):180S–7S. [DOI] [PubMed] [Google Scholar]
[70].Mazzuco R, Hexsel D. Poly-L-lactic acid for neck and chest rejuvenation. Dermatol Surg. 2009;35:1228–37. [DOI] [PubMed] [Google Scholar]

